【技术深耕】肿瘤免疫实验全流程避坑指南:从样本处理到成像的实战方法论
三年前第一次独立操作免疫组化实验时,我在暗室盯着那片蓝不蓝绿不绿的切片发呆。背景像被撒了一层雪花,目标信号却若隐若现。那一刻才真正理解什么叫「实验玄学」——同样的步骤,换个时间做结果就完全不同。
从源头说起:样本处理决定了实验天花板
组织固定是免疫组化的第一道关卡。甲醛渗透不均匀会导致抗原封闭,过度固定则让表位彻底变性。我后来养成习惯:取样后30分钟内完成固定,4%多聚甲醛+室温+6-8小时的组合经过无数次验证。脱水透明浸蜡环节,温度绝不能超过58℃,石蜡渗透不良的组织块切出来的片子,抗体根本进不去。
抗原修复:决定信号强度的关键变量
高温高压修复是我最推荐的方案。pH6.0柠檬酸盐缓冲液+121℃+15分钟的参数,能让90%以上的靶点恢复活性。但要注意:修复液必须现用现配,重复使用会导致pH漂移,直接影响修复效果。部分核内抗原则需要蛋白酶K消化,20μg/mL+37℃+10分钟的参数相对稳妥。
抗体选择与验证:不踩坑的核心原则
单克隆抗体特异性优于多克隆已成共识,但并非绝对。我通常要求供应商提供详细的染色图谱和文献引用。稀释比例需要梯度测试,1:50到1:500之间找到最优浓度——信号清晰且背景干净才是金标准。一抗4℃过夜孵育,二抗37℃1小时的组合,信号强度比室温2小时方案稳定30%以上。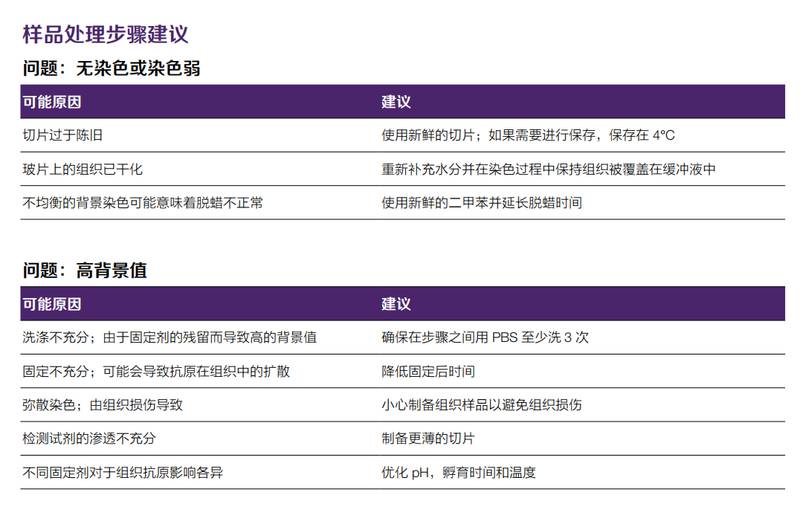
多重检测与空间生物学:突破维度限制
传统DAB显色只能做单指标,想要多靶点同步解析必须上多重荧光方案。Opal多重荧光染色技术配合光谱成像,单张切片可实现7-9个标志物同时检测。关键参数:TSA信号放大后需要彻底去除未反应染料,否则会产生严重串扰。Opal540/570/650/780四色组合,覆盖常见免疫细胞marker搭配组合。
自发荧光去除:被忽视的信号杀手
老化组织、缺血样本的自发荧光往往比目标信号还强。488nm激发通道受影响最大,Cy3/Cy5长波长方案可有效规避。自发荧光光谱分离算法如SpectralUnmixing,配合Imaris或InForm软件处理,能将信噪比提升2-3个数量级。苏木精复染后用乙醇分化可同时去除红细胞自发荧光,这个细节很多人不知道。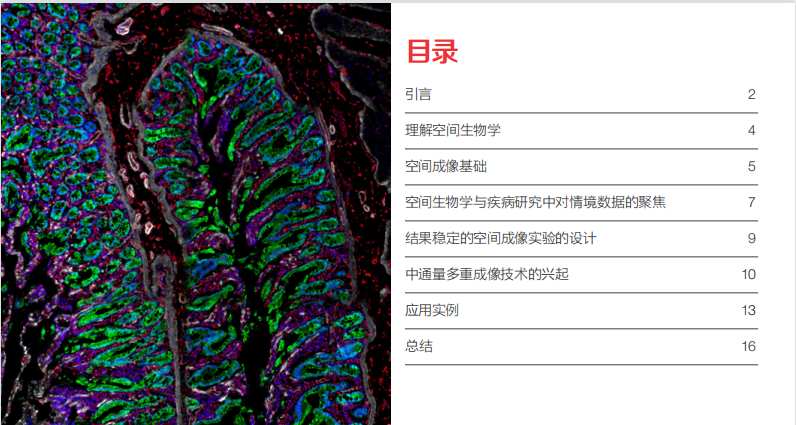
数据可重复性:建立标准化流程
批次间差异是IHC的老大难问题。我的解决方案:设立阳性对照、阴性对照和内参三组质控样本,每批次实验同步运行。采用自动化染色平台可降低80%的人为操作误差,Ventana、LeicaBond系列都是经过验证的选择。原始数据保存原始.tiff格式,勿压缩勿调整亮度对比度,这是后续溯源的基础。
